| 4 декабря 2008 года Тералоку (нимотузумабу) отказано в регистрации в Европе (EMEA/645579/2008)
4 декабря 2008 года Тералоку (нимотузумабу) отказано в регистрации в Европе (EMEA/645579/2008)
4 декабря 2008 года Тералоку (нимотузумабу) отказано в регистрации в Европе (EMEA/645579/2008)
Европейское агентство лекарственных препаратов (EMEA) получило официальное уведомление от компании Oncoscience AG, Германия, о решении отозвать свою заявку на получение регистрационного свидетельства для препарата Тералок (нимотузумаб) - концентрата 5 мг/мл для внутривенной инфузии, который производится в Индии.
Ожидалось, что препарат Тералок будет зарегистрирован в Европе для лечения детей и юношей с рецидивной или резистентной к лечению глиомой низкой степени дифференциации. Ранее, 2-го сентября 2004 года, Тералок получил статус препарата, имеющего ограниченный рынок (orphan designation) и агенством EMEA было разрешено проводить клинические исследования с участием препарата при раке поджелудочной железы.
Заявка на разрешение регистрации препарата Тералок была подана в EMEA 4-го октября 2007 года. На момент отзыва заявка находилась на стадии рассмотрения в комитете по лекарственным продуктам для использования у людей (CHMP).
В своем официальном письме компания заявила, что заявка была отозвана в связи с тем, что компания не могла адекватно ответить на вопросы CHMP относительно качества и эффективности лекарственного средства. Вопросы EMEA относительно эффективности нимотузумаба основаны на данных, представленных в EMEA и полученных компанией Oncoscience AG в неспланированном ретроспективном подгрупповом анализе одногруппового открытого исследования монотерапии II фазы, осуществленного на материале 47 педиатрических пациентов с глиомой. Исследование не отвечало стандартам доказательной медицины, поэтому и не явилось убедительным для возможной регистрации препарата Тералок в Европейских странах.
Два года назад, 28 декабря 2006 года биотехнологическая компания Biocon Ltd, Индия, которая производит нимотузумаб (BIOMAB-EGFR), подала результаты постмаркетингового исследования (ПМИ) противоракового препарата BIOMAB-EGFR (нимотузумаба) для лечения рака головы и шеи на включение их в базу данных клинических исследований в США. В этой базе данных, пополняемой консорциумом компаний, собраны результаты клинических исследований о безопасности и эффективности новых препаратов. Главный менеджер по вопросам развития бизнеса в компании д-р Субир Басак считает, что: "рак головы и шеи не изучен в США, тогда как на Индийском субконтиненте регистрируется около одной трети случаев с раком головы и шеи в мире. Результаты ПМИ станут полезными для исследований рака во всем мире>. <В США скептически относятся к моноклональным антителам, произведенным в Индии. Результаты ПМИ нового препарата станут сигналом пробуждения для скептиков," добавил д-р Басак.
Тем не менее, в настоящее время в США, Японии, Европейских странах и Германии Тералок (нимотузумаб) не зарегистрирован для лечения пациентов в силу отсутствия доказательств эффективности и безопасности препарата в рандомизированных клинических исследованиях III фазы
По материалам сайтов:
http://www.emea.europa.eu/
http://www.oralcancerfoundation.org/news/story.asp?newsId=1566
http://cancer.immunodefence.com/2006/12/biocon-to-file-cancer-drug-res.html#more
|
|













 Роль антитромботической терапии при хронической сердечной недостаточности (ХСН) у пациентов с синусовым ритмом обсуждается много лет. В частности, оживленные дискуссии вызывает воп..
Роль антитромботической терапии при хронической сердечной недостаточности (ХСН) у пациентов с синусовым ритмом обсуждается много лет. В частности, оживленные дискуссии вызывает воп..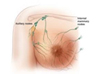 Пожилой возраст является фактором риска при раке молочной железы (РМЖ). Большая часть смертей от РМЖ происходит именно у пожилых. Не всегда у них удается провести лечение сог..
Пожилой возраст является фактором риска при раке молочной железы (РМЖ). Большая часть смертей от РМЖ происходит именно у пожилых. Не всегда у них удается провести лечение сог.. Международная Организация Гражданской Авиации\International Civil Aviation Organisation подсчитала, что во время авиакатастроф пассажирских самолетов, происходивших в 1930-е годы,..
Международная Организация Гражданской Авиации\International Civil Aviation Organisation подсчитала, что во время авиакатастроф пассажирских самолетов, происходивших в 1930-е годы,.. Жаропонижающие лекарственные средства - препараты, наиболее часто используемые для лечения детей как педиатрами, так и родителями. Этому способствуют бытующие представления об опас..
Жаропонижающие лекарственные средства - препараты, наиболее часто используемые для лечения детей как педиатрами, так и родителями. Этому способствуют бытующие представления об опас.. За последние два десятилетия были изучены генетические основы различных форм кардиологических заболеваний и достигнуто лучшее понимание причин данных патологических нарушений, их м..
За последние два десятилетия были изучены генетические основы различных форм кардиологических заболеваний и достигнуто лучшее понимание причин данных патологических нарушений, их м..
 Новости
Новости 